

“Rapid Access to Kinase Inhibitor Pharmacophore by Regioselective C–H Arylation of Thieno[2,3-d]pyrimidine”
Shuya Yamada, Kayin Nicole Flesch, Kei Murakami,* Kenichiro Itami*
Org. Lett. 2020, Accepted. DOI:10.1021/acs.orglett.0c00143.
アリールチエノ[2,3-d]ピリミジン骨格はプリン塩基との構造類似性から、キナーゼをターゲットとした抗がん剤開発で見られる重要なファーマコフォアである。今回我々は、パラジウム触媒を用いてチエノ[2,3-d]ピリミジンに対する位置選択的なC–Hアリール化反応を開発した。本反応でチエノ[2,3-d]ピリミジンは、ヨウ化アレーンと6位選択的に、アリールボロン酸と5位選択的にカップリングし、対応する種々のアリールチエノ[2,3-d]ピリミジンへと変換された。また、開発した触媒を用いることでキナーゼ阻害剤の短工程かつ多様性指向型合成を達成することができた。本手法は化合物ライブラリーの構築を大きく加速させるものであり、創薬研究での応用が期待される。
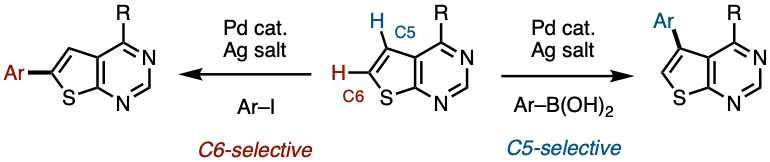
Aryl thieno[2,3-d]pyrimidine, which is structurally similar to the purine base, is a significant pharmacophore in the development of kinase inhibitors toward anticancer drugs. In this article, the palladium-catalyzed regioselective C–H arylation of thieno[2,3-d]pyrimidine is described. The coupling reaction proceeded with aryl iodides at C6 position while with arylboronic acids at C5 position regioselectively to provide the corresponding aryl thieno[2,3-d]pyrimidines. Synthetic advantage of the developed protocol was highlighted by demonstrating rapid and divergent synthesis of kinase inhibitors. This methodology would accelerate the chemical library construction, which will be beneficial in the field of drug discovery.